нет ответа яичников на стимуляцию (эко)
Эко после 38 лет с плохим ответом на стимуляцию. возможно ли эко при менопаузе?
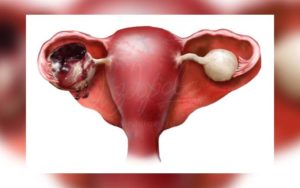
Откладывание рождения ребенка на более поздний период приводит к тому, что в момент, когда женщина уже готова, ее репродуктивные возможности весьма ограничены. Даже при обращении в репродуктивную клинику результата добиться сложно.
ЭКО после 38 лет сопряжено со многими трудностями: плохим ответом яичников на стимуляцию, резким снижением запаса яйцеклеток, появлением соматических болезней, плохим качеством яйцеклеток и генетической неполноценностью эмбрионов.
Второй рассматриваемый вопрос в статье – это возможность проведения ЭКО при климаксе.
- Почему после 38 сложно забеременеть
- ЭКО после 38 лет
- Прогнозы на исход
- Бедный ответ на стимуляцию яичников
- Влияние возраста на генетическое состояние ооцитов
- Хромосомные аномалии у бластоцист
- Виды протоколов ЭКО после 38 лет при плохом ответе яичников на стимуляцию
- Накопление ооцитов или эмбрионов
- Медикаментозная подготовка
- Возможно ли ЭКО при климаксе: необходимые условия
- Донорские программы и суррогатное материнство
Почему после 38 трудно забеременеть
С возрастом увеличивается количество факторов, снижающих фертильность:
- Учеными фиксируется более высокая частота гинекологических заболеваний. Чаще всего после 38-39 лет женщины сталкиваются с такими проблемами: эндометриоз, лейомиомы, гиперплазии и полипы в матке и шейке матки.
- Нарушения имплантации эмбрионов и развитие биохимических беременностей, которые прерываются на ранних сроках.
- Ухудшение общего и репродуктивного состояния здоровья влекут за собой высокий риск невынашивания беременности.
- Чем старше женщина, тем выше риски акушерских осложнений и неблагоприятных исходов беременности.
Почему в возрасте после 38 лет ЭКО вызывает сложности
Протокол ЭКО подразумевает собой стимуляцию роста и развития яйцеклеток. Полный путь развития фолликула занимает 112-185 дней. Количество фолликулов, созревающих в цикле, зависит от возраста.
| Возраст | Количество антральных фолликулов в 1 цикле в обоих яичниках |
| 25 лет | 35 |
| 35 лет | 10 |
| 45 | Не превышает 2-3 |
Ключевым моментом при проведении ЭКО после 38-39 лет является оценка овариального резерва – количества яйцеклеток, потенциально пригодных к оплодотворению.
На снижение запаса яйцеклеток влияют:
- генетические факторы;
- хирургические операции на яичниках;
- аутоиммунные процессы, в том числе и эндометриоз;
- лучевая и химиотерапия;
- курение;
- особенности внутриутробного развития женщины (влияние негативных факторов во внутриутробном периоде во время закладки половых клеток у плода);
- возраст и вес пациентки.
Прогнозируемые исходы лечения бесплодия методом ЭКО у женщин старше 38 лет
Для проведения ЭКО после 38 прогнозы на успех строятся исходя из результатов комплексного обследования. Для этого проводится:
- Подсчет количества антральных фолликулов по данным ультразвукового обследования (УЗИ).
- Определяется уровень антимюллерова гормона (АМГ) – наиболее важный маркер. Уровень ингибина B в крови – менее важен, так как зависит от размера фолликулов. Показатель может отображать норму при наличии функциональных кист.
- На 2-3 день МЦ исследуется концентрация ФСГ и эстрадиола. Это также важные показатели, но на их уровень влияет прием препаратов.
- Оценивается возраст и длительность менструаций. Снижение ОР предполагают у женщин после 38 лет, которые отмечают укорочение менструального цикла – менструации наступают более часто.
- Наличие оперативных вмешательств на яичниках в анамнезе. Резекция яичников подразумевает удаление части тканей органа, а вместе с ней преморбидных фолликулов, из которых развиваются антральные.
- Объем яичников по данным УЗИ.
Все эти показатели и факторы предсказывают количество фолликулов, а не качество яйцеклеток, что более важно для результата искусственного оплодотворения.
Плохой ответ на стимуляцию при проведении ЭКО после 38
Международные критерии низкого ответа на стимуляцию:
- Возраст старше 40 лет.
- Получение 3 и менее ооцитов в предыдущих протоколах ЭКО со стандартной стимуляцией.
- АМГ меньше 0,5-1,1 нг/мл. Уровень меньше 0,086 нг/мл четко соответствует началу времени перехода организма к менопаузе. Сам предменопаузальный период может длиться 4-5 лет.
- Менее 5-7 антральных фолликулов в обоих яичниках.
Одной из причин плохого ответа на стимуляцию является изменение чувствительности рецепторов ФСГ и ЛГ. Эти изменения генетически обусловлены и являются причиной преждевременного истощения яичников.
Бедный ответ яичников может быть и у молодых женщин, что обусловлено генетически или по другим причинам.
Возраст – основной фактор вероятности наступления беременности в циклах ЭКО
На исход ЭКО после 38 лет влияет не только запас яйцеклеток, но и их генетическая полноценность. Доказано, что частота эуплоидных эмбрионов (с правильным набором хромосом) в 30 лет составляет 70%.
С возрастом показатель снижается и достигает практически 0 к 45 годам. После 35 лет эмбрионы с хромосомными нарушениями преобладают над эуплоидными.
Естественно, что к 38 годам соотношение смещается в сторону эмбрионов с патологическим хромосомным набором.
Корреляция хромосомных нарушений у эмбрионов с возрастом женщины
С возрастом ухудшается качество бластоцист в генетическом отношении, отсюда потери беременностей в протоколах ЭКО. Такие бластоцисты, даже если имплантация происходит, обречены. А для женщины — это потерянные беременности и низкий процент успеха в циклах экстракорпорального оплодотворения.
| Количество ооцитов | Бластоцисты с хромосомными нарушениями (%) | |||
| Доноры | Менее 35 лет | 35-39 лет | 40-42 года | Более 42 лет |
| 30% | 40% | 50% | 70% | 85% |
Исходя из этого можно подсчитать необходимое количество ооцитов для успешного ЭКО.
| Возраст | Зрелых ооцитов | Оплодотворенных яйцеклеток | Количество бластоцист | Количество бластоцист с нормальным хромосомным набором | Доля эуплоидных в % |
| До 35 лет | 5 | 4 | 2 | 1 | 60% |
| 39-40 лет | 9 | 7 | 3 | 1 | 30% |
| 42-43 года | 16 | 13 | 5 | 1 | 20% |
В 38-39 лет необходимо получить 9 зрелых ооцитов, чтобы получить 1 бластоцисту с правильным набором хромосом. А учитывая бедный овариальный ответ на стимуляцию это достаточно сложно. Конечно, бывают протоколы ЭКО у женщин после 40 лет с положительным исходом с первого раза и с собственной яйцеклеткой, но это, скорее, исключение.
Виды протоколов ЭКО, используемых у женщин после 38 лет с плохим ответом на стимуляцию
Ни один из протоколов ЭКО, существующих на сегодняшний день, для женщин старшего репродуктивного возраста не показал своего преимущества. Поэтому врач самостоятельно выбирает тот протокол, который посчитает нужным, исходя из данных обследований и анализов.
Доказана эффективность добавления в схему протокола экстракорпорального оплодотворения препаратов ЛГ (Менопур, Мерионал) до начала стимуляции (в предшествующем цикле ЭКО) в когорте пациенток после 38-39 лет.
Чаще других используются протоколы с антагонистами ГнРГ (Оргалутран, Фирмагон, Цетротид). Для них характерно повышение стартовых доз препаратов ФСГ с целью получения большего количества ооцитов. Индивидуально могут назначаться адъюванты – препараты для снижения ФСГ в предшествующем цикле. Чаще всего для этой роли применяют препараты эстрогена – Прогинова, Дивигель.
Стараются использовать и альтернативные схемы:
- Минимальную стимуляцию (начинают с клостилбегита или летрозола, с последующим введением препаратов фолликулостимулирующего гормона);
- Двойная стимуляция – за 1 цикл стимулируют яичники дважды, что позволяет накапливать ооциты. По цене этот протокол будет дороже, так как цена состоит из суммы 2 протоколов, но есть возможность сэкономить время и получить желаемый результат.
Также существует программа, в которую желающих перейти мало, но эффективность ее гораздо выше – это донация ооцитов. Ее рекомендуют, когда не получается собрать собственные яйцеклетки или их качество низкое.
Накопление ооцитов или эмбрионов
Затратная процедура, но с научным обоснованием – это накопление яйцеклеток или эмбрионов. Накапливать эмбрионы перспективней, чем ооциты. Бластоцисты лучше переносят разморозку после криоконсервации. После 38 лет при неудачной попытке имеет смысл задуматься о накоплении эмбрионов. После 40 для получения 1 пригодной к переносу бластоцисты необходимо получить 17-18 ооцитов.
В ходе исследований была показана статистическая достоверность увеличения частоты живорождений в группе накопления эмбрионов, что составило 36% против 23% в группе без накопления.
Медикаментозная подготовка к протоколу ЭКО после 38 лет
Подготовка также всегда индивидуальна. Существует несколько вариантов, выбор какой из них применить зависит от опыта врача и показаний.
После 38 лет при проведении ЭКО могут назначаться схемы препаратов и вспомогательные методы лечения:
- Назначение андрогенов дает возможность увеличить количество антральных фолликулов. Препараты андрогена не могут повысить качество ооцитов, но за счет увеличения количества можно «попасть» на зрелую и полноценную яйцеклетку. Такое лечение имеет место быть, если уровень тестостерона в крови снижен. Если тестостерон в норме, то применение этой группы препаратов менее целесообразно.
- Применение эстрогенов в лютеиновой фазе. Если на УЗИ определяют, что фолликулы растут неравномерно, то до стимуляции назначаются препараты группы эстрогена с 20-21 дня цикла и позже.
- Назначение ХГЧ и ЛГ для увеличения количества ооцитов.
- Для созревания эндометрия и полноценного проникновения гормонов в яичники назначается терапия, направленная на улучшение микроциркуляции (Актовегин, Курантил, Гепарин).
- Имеет место быть заместительная терапия – ЗГТ, так как в нее входят эстрогены.
При необходимости рекомендуют физиотерапию, фитотерапию, приведение веса к норме, и обязательный отказ от курения.
Эко при менопаузе
Группа старшего репродуктивного возраста часто задает вопросы касательно экстракорпорального оплодотворения при климаксе.
ЭКО в менопаузе делают при соблюдении таких требований:
- отсутствуют противопоказания к проведению ЭКО, процедуре переноса эмбрионов;
- нет противопоказаний к гормональной терапии;
- состояние матки и организма в целом позволяет выносить беременность самостоятельно. Матка должна быть нормальных размеров, без миоматозных узлов и деформаций.
Во время климакса матка уменьшается, поэтому для наступления беременности в протоколе ЭКО важно, чтобы не было атрофии органа. Если за счет заместительной гормональной терапии ее удается вернуть к физиологическому состоянию и репродуктологи получают адекватный ответ эндометрия, то ЭКО можно сделать.
Необходимо помнить, что собственных яйцеклеток у женщины во время наступившего климакса уже нет. Поэтому супружеская пара должна быть готова к проведению ЭКО с донорскими ооцитами.
Донорские программы и суррогатное материнство
Донорские программы экстракорпорального оплодотворения (донация яйцеклеток или эмбрионов) порой являются единственным шансом стать родителями. При здоровой матке вероятность успеха выше 70%.
ЭКО с донорской яйцеклеткой
В рассматриваемой возрастной группе иногда приходится обращаться к программам с суррогатного материнства. К ним обращаются, если есть возможность зачать генетически родного ребенка, но нет возможности выносить его:
- отсутствие матки (врожденное или приобретенное);
- деформации полости матки или шейки при врожденных пороках развития или в результате перенесенных болезней;
- патология эндометрия (сращение, синехии, атрофия);
- беременность противопоказана при общих заболеваниях организма;
- 3 и более неудачных попыток ЭКО с переносом эмбрионов хорошего и отличного качества;
- привычное невынашивание (3 и более самопроизвольных выкидыша в анамнезе).
Существует возможность проведения программ с анонимным суррогатным материнством. Суррогатная мать не может быть одновременно донором ооцитов – это запрещено законом.
Светлана Стас
Что происходит с эмбрионом после переноса в матку
Беременность при миоме матки
Классификация эмбрионов по качеству
Как вести себя после переноса эмбрионов
Развитие эмбриона до переноса: ЭКО под микроскопом
Что такое криопротокол и его преимущества
ЭКО после 40 лет
Почему эмбрион не приживается после ЭКО
Процедура донорства яйцеклетки
Чем занимается эмбриолог и что это за доктор
Источник: https://stanumamoy.com.ua/eko-posle-38-let-i-plohoy-otvet-na-stimulyatsiyu/
Овариальный резерв яичников
Под овариальным резервом яичников понимают функциональный резерв, который определяет способность яичников к развитию здорового фолликула с полноценной яйцеклеткой.
Овариальный резерв отражает количество находящихся в яичниках фолликулов (примордиальный пул и растущие фолликулы) и зависит от многих факторов, влияющих как на количественные параметры фолликулярного аппарата, так и на регуляцию фолликулогенеза.
Таким образом, овариальный резерв является важнейшей составляющей репродуктивного потенциала женщины.
- концентрация ФСГ (фолликулостимулирующего гормона) в крови (сдаётся на 2-3 день менструального цикла);
- АМГ (анитмюллеров гормон) в крови (сдаётся на любой день менструального цикла);
- число фолликулов (от 2 до 10 мм в диаметре) и общий объем яичников – во время процедуры УЗИ;
- ингибин В в крови (сдаётся на 2-3 день менструального цикла).
В целом, возраст можно считать надежным фактором качества ооцитов, а уровень ФСГ – маркером собственно фолликулярного резерва.
Выделяют следующие клинические значимые границы концентрации ФСГ, определяющие характер ответа на ФСГ-содержащие препараты:
- 3-8 МЕ/л – норма: предполагается хороший ответ на стимуляцию;
- 8-10 МЕ/л – ответ может колебаться от нормального до умеренно сниженного;
- 10-12 МЕ/л – низкий овариальный резерв, сниженный ответ на стимуляцию;
- 12-17 МЕ/л – плохой ответ на стимуляцию и низкая частота наступления беременности;
- Больше 17 МЕ/л – очень плохой ответ на стимуляцию.
Также практически значимым маркером фолликулярного резерва, является определяемое с помощью УЗИ на 2-3 день менструального цикла число фолликулов до 10 мм в диаметре:
до 5 фолликулов – предполагается «бедный ответ» на стимуляцию, высокий риск отмены цикла стимуляции; от 5-7 фолликулов – возможен «бедный ответ», требуется более высокая стартовая и курсовая доза ФСГ; 8-12 фолликулов – умеренный ответ, умеренные стартовые и курсовые дозы ФСГ для стимуляции; 13-20 фолликулов – хороший ответ на небольшие стартовые и курсовые дозы ФСГ, умеренный риск СГЯ; более 20 фолликулов – чрезмерный ответ, высокий риск СГЯ (синдром гиперстимуляции яичников).
Ингибин В – гормон, у женщин синтезируется в гранулезных клетках, растущих антральных фолликулов, у мужчин – в семенных канальцах яичка (клетках Сертоли). Ингибин В подавляет секрецию ФСГ. В репродуктивном периоде во время фолликулярной фазы цикла уровни ингибина В и ФСГ обратно пропорциональны.
Таким образом, уровень ингибина В отражает состояние овариального резерва, что позволяет использовать показатель для прогнозирования характера ответной реакции (адекватная или ослабленная) яичников на гонадотропины.
Антимюллеров гормон (АМГ) является представителем трансформирующих факторов роста и у млекопитающих играет важную роль в эмбриогенезе особи мужского пола. Он продуцируется клетками Сертоли и вызывает регресс органов мюллерова протока (маточных труб, матки и верхней части влагалища).
У женщин АМГ вырабатывается в преантральных и малых антральных фолликулах (менее 4 мм), в фолликулах большего размера продукция гормона резко снижается и почти не определяется при достижении фолликулом размера 8 мм и более.
Если ингибин В и эстрадиол являются ФСГ-зависимыми по принципу отрицательной обратной связи, то продукция АМГ не зависит от уровня ФСГ и не меняется в течение менструального цикла.
Норма АМГ – от 1,0 до 2,5 нг/мл.
Слабый («бедный») ответ на стимуляцию
Проблема слабого ответа («бедного ответа») яичников на стимуляцию гонадотропинами в программах ЭКО у женщин репродуктивного возраста волнует специалистов на протяжении длительного времени.
Актуальность данной проблемы обусловлена, прежде всего, увеличением числа женщин старшего репродуктивного возраста (после 35-38 лет), обращающихся в центры ЭКО с целью лечения бесплодия.
Доля таких пациенток составляет – 40 %.
«Бедный (низкий, плохой) ответ» – это недостаточная реакция яичников на введение даже больших доз (более 300МЕ/сут) гонадотропинов, когда в схемах стимуляции применяемых циклах программы ЭКО, не удается обеспечить роста и созревания более 3 фолликулов.
Яичники являются не только органом, в котором образуются половые гормоны, но и «банком» пула (запаса) фолликулов.
Ведущим прогностическим признаком при оценке их функционального состояния и критерием успешного лечения бесплодия является способность яичников отвечать на стимуляцию гонадотропинами (ГТ) созреванием адекватного числа фолликулов.Этот ответ со стороны яичника отражает так называемый «овариальный резерв», который в основном зависит от исходной величины пула примордиальных фолликулов.
Пул ооцитов в процессе жизни женщины не восполняется и является индивидуальной величиной, достигающей пика к 3-4-му месяцу гестации (около 7 миллионов). Затем происходит сокращение количества фолликулов вследствие процессов апоптоза (гибели) от 1 миллиона при рождении девочки до 250 000-300 000 в период менархе (к началу первой менструации).
Процесс «истощения» фолликулярного аппарата происходит постоянно, усиливаясь к концу репродуктивного периода – после 37 лет (т.е. за 10 и более лет до наступления менопаузы).
К этому моменту в яичниках остается примерно 25 000 фолликулов, а к перименопаузе – всего около 1 000.
Лишь 300-400 фолликулов овулируют от момента менархе до наступления менопаузы, остальные подвергаются атрезии (исчезновению).
Гормонально-независимый этап развития фолликула длится от 180 до 300 суток. Развитие фолликулов на этом этапе обеспечивается внутрияичниковыми факторами; количество «проснувшихся» фолликулов, а также доля фолликулов, подвергающихся атрезии, не зависят от индукторов овуляции и уровня гонадотропинов в крови.
Ооциты из начавшего роста пула 30-300 фолликулов обречены либо на атрезию, либо на овуляцию. Механизмы атрезии и апоптоза обеспечивают выживание наиболее перспективных фолликулов и, возможно, селекцию генетически здоровых ооцитов.
По достижении частью фолликулов определенных размеров начинается гормонально-зависимая фаза. Происходит селекция и рост доминантного фолликула, что зависит от концентрации гонадотропинов (ФСГ и ЛГ) и многих внутрияичниковых регулирующих субстанций.Таким образом, расход запаса фолликулов и ооцитов происходит по законам внутрияичниковой регуляции и не зависит от применения индукторов овуляции.
Индукторы овуляции влияют на уже зреющие фолликулы, дошедшие до стадии селективных, не затрагивая примордиальных. Индукторы овуляции не способствуют истощению фолликулярного резерва, снижению фертильности, приближению возраста менопаузы.
Не подлежит сомнению, что в программе ЭКО лишь большое число получаемых фолликулов (8-12) и, как следствие, ооцитов (6-10) и эмбрионов (5-8) позволяет отобрать для переноса наилучшие по качеству эмбрионы, соответствующие классу А (или хотя бы классу В). У пациенток с «бедным ответом», при общем числе получаемых эмбрионов эта задача становится фактически неразрешимой.
На практике это приводит к тому, что приходится использовать для переноса эмбрионы, не выбранные в качестве лучших, а «те, что есть» или вообще прервать лечебный цикл при наличии в них очевидных дефектов раннего эмбриогенеза.
При слабом («бедном») ответе отбор ооцитов и эмбрионов основывается не на показателе их качества, а лишь на характеристике жизнеспособности, что снижает эффективность лечения.
Старение как причина снижения репродуктивного потенциала и как фактор риска «бедного ответа» в программе ЭКО
В биологическом отношении старение универсально и неизбежно. Скорость процессов старения репродуктивной системы определяется взаимодействием между генетическими факторами и многообразными влияниями окружающей среды.
Окончательному угасанию репродуктивной функции, т.е. менопаузе, предшествует поздний репродуктивный период, в котором отмечается прогрессирующее снижение функции яичников. Его характерными особенностями являются увеличение частоты ановуляторных циклов, изменение длительности менструального цикла и количества крови, теряемой во время менструации.
Гормональная функция яичников прекращается в возрасте менопаузы, приблизительно в 50 лет, а способность к зачатию исчезает у женщин гораздо раньше – в среднем после 40 лет.
Причины «бедного ответа» не связанные с возрастом
У молодых женщин функция яичников может быть потеряна вследствие преждевременного истощения (недостаточности) яичников, их оперативного удаления или обширной двухсторонней резекции, приведшей к развитию посткастрационного синдрома.
Основные причины развития преждевременной недостаточности яичников без хирургического вмешательства:
- Наличие врожденной дисгенезии гонад, которая обычно связана с синдромом Шерешевского-Тернера;
- Аутоиммунная агрессия против антигенов яичника;
- Ферментативные дефекты;
- Генетические дефекты;
- Химиолучевая и другая гонадотоксичная терапия.
Развитие в последние годы технологий криоконсервации ооцитов позволяет обеспечивать сохранение генетического материала для дальнейшего деторождения.
Также необходимо указать на некоторые причины, приводящие к ослаблению чувствительности яичников, которые могут иметь место у молодых женщин:
- Резекция яичников (одного или обоих);
- Повторные операции на органах малого таза (даже без резекции яичников);
- Аутоиммунный тиреоидит и гипотиреоз;
- Сахарный диабет, заболевание почек, коллагенозы;
- Наружный генитальный эндометриоз;
- Идиопатическое бесплодие;
- Первичное и вторичное бесплодие, обусловленное гипогонадотропной аменореей.
Программы ЭКО, используемые для профилактики «бедного ответа»:
- «Короткий» протокол с аГн-РГ
- «Короткий» протокол с микродозами аГн-РГ
- «Длинный» протокол с низкими дозами аГн – РГ
- Модифицированный протокол с анти Гн-РГ
- Комбинированное введение аГн-РГ и антиГн-РГ
- Мягкие протоколы:
- протокол с кломифен цитратом (КЦ) в комбинации с гонадотропинами и анти Гн-РГ;
- протокол с минимальной стимуляцией гонадотропинами в комбинации с анти Гн-РГ.
- ЭКО в естественном цикле
Выбор протокола стимуляции функции яичников – строго индивидуален.
Стоимость обследований
Все услуги
| ФСГ (фолликулостимулирующий гормон) (кровь(сыворотка), срок дни — 1) | 390 руб. |
| Антимюллеровский гормон (АМГ) (кровь(сыворотка), срок дни — 1-3) | 1 260 руб. |
| Ингибин-B (кровь(сыворотка), срок дни — до 7) | 1 260 руб. |
| УЗИ органов малого таза | 2 500 руб. |
| Ультразвуковая фолликулометрия | 900 руб. |
Источник: http://www.VitroClinic.ru/diagnostika-besplodiya/diagnostika-zhenskogo-besplodiya/ovarialnyy-rezerv-yaichnikov/
Эко с одним яичником
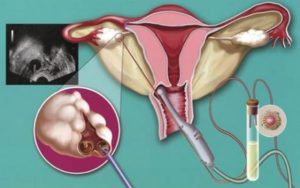
С каждым годом, не смотря на все усилия врачей внедрять профилактическую медицину, к сожалению, растет заболеваемость многими нозологическими формами. И, конечно же, не исключением является репродуктивная сфера женского организма. Одними из наиболее частых патологий в гинекологии считаются заболевания яичника.
Некоторые патологические процессы поддаются грамотно назначенному, консервативному лечении, а в некоторых случаях единственным выходом является применение радикальных операций, суть которых составляет удаление пораженного органа. В данном случае яичника.
Операции по удалению яичника называют овариэктомией, а если яичник удаляется совместно с маточной трубой – аднексэктомией.
Причины удаления яичника
Какие же причины могут заставить докторов пойти на операцию по удалению одного яичника?
Тубоовариальное образование (тубоовариальный абсцесс) – гнойно -воспалительный процесс яичника, который вовлекает как маточную трубу, так и яичник. Представляет собой общих конгломерат, наполненный гнойным содержимым. Единственным способом, который позволит избежать септических состояний при таком диагнозе – это радикальная операция.
- Перекрут кисты яичника, который достиг стадии некроза так же является показанием к удалению на уровне хирургической ножки.
- Разрыв кисты яичника. При такой нозологической форме конечно же есть возможность все-таки сохранить такой важный орган. Но возникают такие ситуации, при которых развивается массивнейшее кровотечение и не всегда врачам удается остановить его консервативным путем.
- Эктопическая беременность, а именно яичниковая форма. Это состояние характеризуется прикрепление плодного яйца не в полости матки, как это положено, а на поверхности яичника. Плодное яйцо хорошо васкуляризируется и глубоко прорастает яичник. В таком случае единственным способом является овариэктомия со стороны внематочной беременности.
- Наличие больших эндометриоидных кист, при удалении которых не удается сохранить даже часть яичника.
После таких оперативных вмешательств главным вопросом женщины является «Смогу ли я теперь забеременеть? Могу ли я теперь иметь детей». Эти мысли, порой. Доводят женщин до серьезных депрессивных состояний, справиться с которыми, часто, самостоятельно не представляется возможным.
Это вопрос сугубо индивидуальный и зависит от особенностей конкретного женского организма, состояния оставшегося яичника, его способности к фолликулогенезу.
У части пациенток второй яичник берет на себя компенсаторные функции и работает, так сказать, «за двоих». У женщины не происходит никаких изменений в общем самочувствии, в стабильности овариально-менструального цикла, а так же беременность наступает без каких-либо дополнительных усилий.Однако есть и такие женщины, у которых второй яичник не справляется с обеспечением всех функций, возложенных на него, и начинаются клинические проявления в виде нарушений овариально-менструального цикла, явления гипоэстрогении, которые затрагивают все процессы в организме.
Препятствия на пути к беременности
Почему же женщины с одним яичников встречают на пути к беременности препятствия?
- Осложнения, формирующиеся после проведения оперативного вмешательства в виде спаечного процесса, который может быть причиной бесплодия;
- Сальпингоофорит единственного яичника;
- Наличие в анамнезе трубной беременности и ее пластика со стороны имеющегося яичника;
- Эндометриоидные гетеротопии на единственном яичнике;
- Диагностирование кист различного генеза на яичнике;
- Инфекции, передающиеся половым путем, в особенности гонорея, которая ведет к массивному спаечному процессу;
Встречаются случаи, когда яичник находится в удовлетворительном состоянии, однако, маточная труба непроходима. Либо ее нет вовсе после проведения тубэктомии по поводу внематочной беременности в анамнезе. Наступление беременности в данной ситуации просто невозможно.
Не стоит отчаиваться, так как в настоящее время благодаря методикам вспомогательных репродуктивных технологий. Даже такую печальную ситуацию можно исправить с помощью применения Эко с одним яичником.
Шансы на получение такой желанной беременности с рождением здорового ребенка у женщин с одним яичником практически ни чем не отливаются от таковых наличии обоих яичников, конечно же, при условии их нормального функционального состояния.
Но не всегда семейная пара может себе позволитьь оплатить столь дорогостоящие манипуляции.
На помощь к таким людям пришло государство, которое предусмотрело программу бесплатного проведения протокола экстракорпорального оплодотворения за счет фонда обязательного медицинского страхования (ОМС).
Стоит собрать документы и подать заявку на сайт. Чудеса все-таки случаются и самые заветные мечты воплощаются в реальность.
Эко с одним яичником без труб ничем не отличается от такового с их наличием. Даже наоборот.
Если перед проведением процедуры экстракорпорального оплодотворения не провести операцию лапароскопической тубэктомии, то есть удаление фаллопиевы труб, высок риск получения эктопической, а именно трубной беременности и пролетного протокола экстракорпорального оплодотворения. Поэтому при такой ситуации во избежание нежелательных последствий стоит пойти на их удаление.Какие же отличия могут наблюдаться в проведении протокола экстракорпорального оплодотворения у женщин с единственным яичником?
Единственным моментом, который может повлиять на ход вспомогательных методик репродукции – это ответ яичников на стимуляцию при ЭКО. Он может быть значительно снижен за счет его преждевременного истощения, так как ему приходиться работать с двойным усилием, компенсируя отсутствие второго органа.
Для этого врачи-репродуктологи подбирают специальные усиленные дозы гормональной терапии для стимуляции овуляции единственного яичника.
Но прежде чем это сделать, доктор должен оценить риски и пользу от данной стимуляции. Если причиной удаления яичника послужили его опухолевые процессы, то стимуляция высокими дозами гормонов просто противопоказана.
Что же делать в этом случае? Выход так же есть. Если применение гормональных препаратов невозможно в конкретном случае, то применяется попытка получить яйцеклетки в естественном цикле женщины.
То есть, если цикл овариально-менструальные с присутствием овуляции, которую необходимо обязательно подтвердить биохимическими показателями уровней гормонов, а так же ультразвуковой фолликулометрией, то врач дожидается дозревания фолликула и производит пункцию для осуществления забора яйцеклетки, которая созрела при обычном цикле у женщины. Дальнейший механизм проведения протокола экстракорпорального оплодотворения осуществляется по обычной схеме: оплодотворение полученной яйцеклетки сперматозоидами мужа, культивирование полученного эмбриона и его перенос в полость матки с обязательной поддержкой лютеиновой фазы.
Если же удаление яичника произошло по каким-либо другим причинам, то гормональные препараты для стимуляции овуляции не противопоказаны, это не влияет на забор яйцеклеток для ЭКО.
После стимуляции производится пункция фолликула. Препятствие к проведению данной манипуляции могут стать послеоперационные последствия в брюшной полости в виде серьезного спаечного процесса. Особенно, если операция была проведена на фоне мощного инфекционно-воспалительного процесса, когда послеоперационный период характеризовался гипертермической реакцией.Пункция фолликула – это достаточно трудоемкий и ювелирный процесс, который должен выполнить хирург с большим опытом и высокой квалификацией. Эти спайки в брюшной полости могут существенно затруднить процесс пунктирования.
Если все же, несмотря на все препятствия, яйцеклетки были получены, то дальнейший протокол экстракорпорального оплодотворения проходит без особенностей.
После резекции яичников ЭКО так же выполняется. Но результат зависит от количества резецированной ткани. Если в силу патологических изменений, причиной которых и стала операция, ткань яичника не значительно пострадала и пришлось резецировать небольшую часть яичника, то получить яйцеклетки путем стимуляции при протоколе ЭКО не будет представлять значительных проблем.
А вот, если происходила значительная резекция с одной стороны, а второй яичник был нетронут и имеет неплохой фолликулярный резерв, то ситуация аналогична – применение стимуляции даст желаемый эффект.
Однако, необходимо обязательно посмотреть фолликулярный резерв яичников при помощи определения антимюллерова гормона, чтобы спрогнозировать ответ на стимуляцию.
Если показатели близки к нижним границам, то есть смысл воспользоваться мятежом ЭКО в естественном цикле либо же индивидуально подбирать схем
Можно столкнуться с такой ситуацией, когда у женщины производилась двухсторонняя резекция яичников в большом объеме. Негативные последствия данной ситуации состоят в том, что хоть ни один, ни второй яичники небыли полностью удалены, но их функциональный резерв может быть исчерпан.Цифры антимюллерова гормона могут стремиться к наименьшим показателям. Тогда семейной паре в таком случае просто будет отказано в проведении протокола экстракорпорального оплодотворения. К большому сожалению.
Эко без яичников — истощение яичников
С приходом в нашу жизнь современной репродуктивной медицины и вспомогательных репродуктивных технологий, и эта проблема разрешима.
Сейчас возможны такие методы с такими нозологическими единицами, как эко и истощение яичников, эко без яичников. В таких случаях единственным решением является использование донорских яйцеклеток.
Смысл такой методики заключается в оплодотворении яйцеклеток женщины донора, которым может быть как совершенно незнакомый человек, который сдал свой биоматериал в клинику, либо родственники пациентки. Как зачастую, и случается.
Какие показания существуют для использования данной методики:
- Невозможность получить собственные яйцеклетки женщины: — синдром преждевременно выключения (истощения) яичников; — наличие противопоказаний к стимуляции гормональными препаратами; — наличие синдрома резистентности яичника – отсутствие ответа данного органа на применение гормональной стимуляции; — разнообразные аномалии развития половых органов в виде дизгенезии гонад; — оперативные вмешательства на яичниках в виде двусторонней овариэктомии – удаление яичников с двух сторон;
- Высокий риск генетический аномалий у женщины либо присутствие у самой женщины генетических отклонений с высоким риском наследования.
- Отрицательный результат проведения нескольких протоколов экстракорпорального оплодотворения с собственными яйцеклетками женщины.
Существует два вида проведения протокола экстракорпорального оплодотворения:
- использование в процессе манипуляций свежих, только полученный яйцеклеток без применения к ним каких-либо средств консервации;
- использование яйцеклеток, которые были подвергнуты криоконсервированию – заморозке.
Экстракорпоральное оплодотворение с использованием «свежих» яйцеклеток включает:
- комплексное лабораторно-диагностическое обследование как супружеской пары, так и донора;
- синхронизация фаз овариально-менструального цикла у женщины-донора и у женщины-реципиента. Осуществляется по средствам применения гормональных препаратов.
- Пункция фолликулов женщины-донора для получения донорского биоматериала в виде яйцеклеток;
- Оплодотворение яйцеклеток, полученных в ходе пунктирования, спермой мужа;
- Культивация эмбрионов до трехдневного либо пятидневного возраста;
- Подсадка эмбрионов в полость матки.
Метод витрификации – заморозки яйцеклеток намного удобнее ранее указанного метода. Этот метод значительно отличается от криоконсервации, так при применении последнего нет возможности в длительном содержании биоматериала в замороженном состоянии. А метод витрификаци позволяет это делать.
Суть его состоит в удалении из яйцеклеток воды, так как при заморозке она повреждает клеточные структуры, а вместо нее в клетку вводятся криопротекторы, вещества, защищающие клетку от воздействий низких температур. Сохранность яйцеклеток при таком термическом действии на них составляет около 98%.
Забранные яйцеклетки помещаются в специализированные сосуды, куда подается жидкий азот или его пары. Температурный режим в таких сосудах сохраняется в пределах -196 градусов по Цельсию при хранении в жидком азоте и -180 – в его парах. Этот метод исключает сложную технологию синхронизации циклов донора и реципиента.
Что является дискомфортным для обеих сторон. По статистике количество беременностей, которые наступили в следствии применения данной технологии хранения биоматерила, ничем не отличается от их количества, полученного в следствии применения «свежих» яйцеклеток.
Поэтому применение этой методики оправдано, абсолютно безопасно и удобно для хранения донорского биоматериала, который в последующем будет субстратом для культивирования чьего-то счастья.
Донорский биоматериал хранится в криобанке, если его параметры подошли для донорства, их размораживают, оплодотворяют спермой мужа реципиента и производят подсадку женщине-реципиенту, конечно же, предварительно готовя ее препаратами, поддерживающими лютеиновую фазу. Эмбрион при хорошем исходе имплантируется в эндометрий и начинает свое развитие, женщина вынашивает беременность, рожает и, конечно же, является биологической матерью данного ребенка.
Данная методика позволяет предоставить радость материнства даже тем женщинам, которые уже отчаялись иметь детей.
Подводя итог, стоит сказать о том, что даже женщины, не имеющие яичников по каким-то причинам, имеют шанс на счастливое материнство благодаря достижениям специалистов в области репродуктологии.
Да, эти методики достаточно дорогостоящие, но государство уже позаботилось о семейных парах, которые не в состоянии потянуть финансово показанные им протоколы экстракорпорального оплодотворения, путем запуска программы бесплатного проведения ЭКО за счет фонда ОМС.Оставив заявку на сайте, бесплодная семейная пара становится на шаг ближе к жизни, наполненной такими прекрасными цветами как их дети!
Источник: https://registr-eco.ru/temyi/chto-takoe-eco-ekstrakorporalnoe-oplodotvorenie/eko-s-odnim-yaichnikom.html
Отделение лечения слабого ответа яичников
Количество и качество овоцитов с возрастом снижается, в связи с чем женщинам становится сложнее забеременеть естественным путем, а иногда этого не удается достичь даже с использованием различных вспомогательных репродуктивных технологий.
При проведении процедур ЭКО один из самых главных этапов заключается в стимуляции яичников. В течение периода в 7-12 дней пациентке вводится медицинский препарат для получения нескольких яйцеклеток, которые в последствии будут оплодотворяться.
Количество полученных яйцеклеток и есть так называемый ответ на стимуляцию. Стимуляция проводится для получения необходимого количества овоцитов, которое позволит иметь благоприятный прогноз на эмбрионы.
Как правило, удовлетворительным количеством считается от пяти овоцитов и более.
У пациенток, получающих одну и ту же дозу медикамента, могут наблюдаться различные ответы яичников: в частности, иногда полученное количество овоцитов является столь низким, что это существенно снижает шансы на общий успех.
Следует остановиться на слабом ответе яичников подробнее.
Запросите смету
Что такое резерв яйцеклеток?
Женщины рождаются с полным набором овоцитов на всю свою жизнь. С течением времени эти овоциты расходуются и к наступлению менопаузы их не остается совсем.
Под овариальным резервом понимается количество жизнеспособных овоцитов в женских яичниках на определенный момент. Этот резерв определяет количество яйцеклеток, которые можно получить при процедуре экстракорпорального оплодотворения (ЭКО). Наиболее надежными маркерами для измерения овариального резерва является подсчет антральных фолликулов на УЗИ и анализ на гормон АМГ.
Несмотря на то, что основной причиной слабого ответа яичников на стимуляцию является собственно низкий резерв яйцеклеток, данная проблема может также возникать и у женщин с нормальным резервом.
Откуда возникает низкий резерв яйцеклеток?
Как мы уже говорили, резерв яйцеклеток постепенно уменьшается с возрастом до полного его истощения, поэтому возраст является основным фактором риска низкого резерва. Однако не все женщины одного и того же возраста имеют одинаковый резерв яйцеклеток.
Можно наблюдать существенные различия: некоторые женщины имеют низкий резерв в еще молодом возрасте, а некоторые и после 40 лет имеют нормальный резерв с хорошим ответом яичников на стимуляцию и, соответственно, высоким количеством овоцитов при проведении процедур ЭКО.
Причиной тому, как правило, являются факторы окружающей среды и, в первую очередь, генетика.
Отделение слабого ответа яичников Института Бернабеу наметило несколько линий для научных исследований, которые, среди прочего, позволят составить генетический профиль женщин, расходующих свой резерв яйцеклеток быстрее других.
Почему проблема слабого ответа
яичников
имеет в настоящее время такую важность?
Социальные изменения, произошедшие в последние годы, вынуждают женщин откладывать материнство. После 35 лет ухудшается не только ответ яичников на стимуляцию, но и отмечается существенное прогрессивное снижение качества овоцитов.
Соотношение возраста с резервом яйцеклеток приводит к тому, что все большее и большее количество пациенток сталкиваются со слабым ответом яичников на стимуляцию и, как следствие, с плохим прогнозом при процедурах экстракорпорального оплодотворения.
Именно для таких пациенток со слабым ответом яичников на стимуляцию особенно важно произвести грамотную оценку состояния и выявить оптимальные стратегии для повышения шансов на общий успех.
Независимый отдел исследования слабого ответа яичников на стимуляцию в Институте Бернабеу
Институт Бернабеу бросает этот вызов ограничениям репродуктивной медицины, чтобы помочь нашим пациенткам вынашивать детей с собственными яйцеклетками. Это первое отделение в Испании, занимающееся такими диагнозами как слабый ответ яичников на стимуляцию и имеющее опыт работы с парами со всех стран мира.
Этот мультидисциплинарный отдел под руководством доктора Жоакина Льасера объединяет специалистов из области репродуктивной медицины, молекулярной биологии, генетики и репродуктивной биологии, которые работают с парами и занимаются лечением и проведением исследований с целью создания индивидуальных планов лечения для каждой пациентки.
В чем заключается мультидисциплинарный подход отделения
низкого
резерва яйцеклеток
?
В нашем отделении каждый случай рассматривается отдельно целой группой профессионалов, специализирующихся в данной области.
Наличие отделения низкого резерва яйцеклеток Института Бернабеу позволяет пациенткам пользоваться самыми актуальными инновациями для диагностики и лечения: тесты в специализированных авангардных лабораториях, гинекологическое УЗИ 4D для исследования сосудов яичников и матки, анализ генетических маркеров, матриксная сравнительная геномная гибридизация и другие исследования для разработки индивидуальной стратегии оптимизации возможностей достижения успеха для каждой конкретной пары.
Преимущества Отделения низкого резерва яйцеклеток Института Бернабеу
Наличие лучших профессионалов в области самой передовой диагностики позволяет разрабатывать наиболее эффективные стратегии лечения в каждом конкретном случае.
За последние годы наше отделение разработало и усовершенствовало самые инновационные протоколы стимуляции яичников.
Адъювантная терапия для повышения чувствительности яичников, собственно стимуляция в лютеиновой фазе, сбор витрифицированных овоцитов, использование мягких протоколов – все это внедрено и уже дает обнадеживающие результаты у пациенток, которым в ином случае должны были бы прибегнуть к донорским овоцитам.Опыт работы со сложными случаями позволяет нам также лучше понимать психологическую нагрузку, ложащуюся на пациенток со слабым ответом яичников на стимуляцию, в связи с чем к ним требуется особый подход и особое внимание к их эмоциональному состоянию.
Достижения в области исследований низкого резерва яйцеклеток
Институт Бернабеу и его Отделение слабого ответа яичников на стимуляцию являются пионерами исследований в данной области.
Результатом этого интереса к исследованиям стало получение нашим институтом в 2012 году премии Американского общества репродуктивной медицины (ASRM) за представленные результаты в области генетических полиморфизмов у женщин со слабым ответом яичников на стимуляцию.
Также мы стали первыми в мире создателями концепции прикладной фармакогенетики в стимуляции яичников с введением нового теста под названием IBgen ЭКО.
В настоящее время центральное место в линиях научных исследований занимают три фундаментальных аспекта:
- Изучение генетических факторов, определяющих старение яичников, для разработки модели прогнозов, на основе которых женщины смогут планировать свою репродуктивную жизнь;
- Разработки в области фармакогенетики, дающие возможность составлять индивидуальные протоколы стимуляции в соответствии с генетическим профилем пациенток, что улучшает ответ организма на вводимые гормоны;
- Поиск новых способов стимуляции посредством клинических испытаний на пациентках со слабым ответом яичников на стимуляцию, в частности, изучение лютеиновой фазы
Полное медицинское обследование за 1 день Высокий уровень специализации именно на пациентках со слабым ответом яичников на стимуляцию позволяет в ходе обследования пройти всех специалистов, так, чтобы за один день пациентка смогла получить полную диагностику для анализа всей картины и разработки индивидуального плана лечения. |
Женское обследование:
|
Источник: https://www.institutobernabeu.com/ru/ib/otdelenie-po-lecheniju-slabogo-otveta-jaichnikov/